Introduzione al prodotto
|
Nome del prodotto |
Cat.No. |
Spec. |
|
Kit di estrazione del DNA genomico vegetale MagBind |
G3621-50T |
50T |
Descrizione/Introduzione
Utilizzando sfere magnetiche superparamagnetiche appositamente sviluppate per l'estrazione e la purificazione degli acidi nucleici e un sistema tampone di lisi appositamente ottimizzato, questo kit può estrarre in modo sicuro, rapido ed efficiente DNA genomico ad elevata purezza da 50-100 mg di campioni di tessuto vegetale (come grano, foglie di mais, ecc). Il tessuto vegetale può rilasciare rapidamente il DNA genomico dopo la lisi e rimuovere efficacemente le impurità nel campione, ad eccezione dell'acido nucleico. Questo kit non richiede fenolo, cloroformio e altri reagenti organici e non richiede la centrifugazione in più fasi. Il DNA genomico estratto può essere utilizzato nella successiva reazione PCR, reazione di digestione enzimatica, ibridazione meridionale, RAPD, AFLP, RFLP e molti esperimenti di biologia molecolare convenzionali.
Condizioni di conservazione e manipolazione
L'RNasi A viene spedita con ghiaccio bagnato e conservata a -20 gradi; I restanti reagenti vengono spediti e conservati a temperatura ambiente; La data di scadenza è di 12 mesi.
Contenuto del prodotto
|
Numero componente |
Componente |
G3621-50T |
|
G3621-1 |
Tampone PGL1 |
30 ml |
|
G3621-2 |
Tampone PGL2 |
5 ml |
|
G3621-3 |
BufferGB |
30 ml |
|
G3621-4 |
Buffer GD |
16 ml |
|
G3621-5 |
PW buffer |
24 ml |
|
G3621-6 |
Perline SweMag |
2×1 ml |
|
G3621-7 |
RNasi A |
1 ml |
|
G3621-8 |
Tampone TE |
10 ml |
|
Manuale |
Una copia |
|
Prima di iniziare (leggere attentamente)
1. Se il tampone PGL1 precipita, riscaldarlo a 65 gradi e utilizzarlo quando viene riportato a temperatura ambiente.
2. Prima dell'uso, aggiungere 24 ml di etanolo anidro al tampone GD e 56 ml di etanolo anidro al tampone PW, mescolare bene e utilizzare.
3. Supporto magnetico autonomo.
Protocollo/procedure del test
1. Lisi di campioni di tessuto vegetale:
UN. Lisato + macinatore Cracking di macinazione: (consigliato) Aggiungere in anticipo 50{{10}} μL di tampone PGL1 a una provetta di macinazione priva di nucleasi da 2,0 ml (consigliato HT-200-M) , quindi aggiungere perline in acciaio inossidabile da 3-4 4 mm (consigliato G0104-200G). Successivamente, trasferire rapidamente 50-100 mg di tessuto vegetale fresco o crioconservato nel tubo di macinazione (i campioni di foglie vengono tagliati a 0,5 cm2, le radici e gli steli vengono tagliati a 0,5 cm). Posizionare il tubo di macinazione sul macinino (consigliato KZ-5F-3D) e macinare (procedura di macinazione consigliata: impostare la frequenza su 70 HZ, macinare per 30 secondi ogni volta, ripetendo il processo {{19 }} volte con un intervallo di 5 secondi tra ogni macinatura Se il campione è difficile da macinare, come radici e steli, è possibile aumentare i tempi di macinazione a 30 o più) fino al la macinazione è omogeneizzata (se il tessuto non è completamente omogeneizzato, ciò influenzerà la resa e la qualità del DNA). Dopo la macinazione completa, aggiungere 20 μL di RNasi A al tubo di macinazione, mescolare sottosopra e incubare a 65 gradi per 15 minuti, mescolando sottosopra ogni 5 minuti.
B. Azoto liquid 0,5 cm2, radici e steli vengono tagliati a 0,5 cm) contenenti perle di zirconio da 3~4 3 mm (consigliato G0203-150G) e preraffreddato con azoto liquido. Posizionare il tubo di macinazione sul macinatore (consigliato KZ-5F-3D) (preraffreddare rapidamente l'adattatore in azoto liquido prima di posizionare il tubo di macinazione) e macinare fino a quando non sarà completamente polverizzato (se il tessuto non è completamente macinato in polvere, ciò influenzerà la resa e la qualità del DNA). Quindi aggiungere 500 μL di tampone PGL1 e mescolare bene, aggiungere 20 μL di RNasi A nella provetta di macinazione, mescolare sottosopra e incubare a 65 gradi per 15 minuti, mescolando sottosopra ogni 5 minuti.
C. Azoto liquido + cracking mediante macinazione con mortaio: trasferire rapidamente 50-100 mg di tessuto vegetale fresco o crioconservato in un mortaio preraffreddato con azoto liquido (i campioni di foglie vengono tagliati a 0,5 cm2, le radici e gli steli vengono tagliati a 00,5 cm). Aggiungere azoto liquido e macinare il tessuto con un pestello, aggiungendo continuamente azoto liquido finché non sarà completamente polverizzato (se il tessuto non è completamente macinato in polvere, ciò influenzerà la resa e la qualità del DNA). Trasferire quindi i campioni in polvere in una provetta da centrifuga priva di nucleasi da 1,5 ml contenente 500 μL di tampone PGL1 e mescolare bene. Aggiungere 20 μL di RNasi A nella provetta da centrifuga, mescolare sottosopra e incubare a 65 gradi per 15 minuti, mescolando sottosopra ogni 5 minuti.
D. Azoto liquido + bastoncino di pestello Frantumazione: trasferire rapidamente 50-100 mg di tessuto vegetale fresco o crioconservato in una provetta da centrifuga priva di nucleasi da 1,5 ml preraffreddata con azoto liquido (i campioni di foglie vengono tagliati a 0,5 cm2 , radici e steli vengono tagliati a 0,5 cm). Aggiungere azoto liquido e macinare il tessuto con un pestello, aggiungendo continuamente azoto liquido finché non sarà completamente polverizzato (se il tessuto non è completamente macinato in polvere, ciò influenzerà la resa e la qualità del DNA). Quindi aggiungere 500 μl di tampone PGL1 alla provetta da centrifuga e mescolare bene. Aggiungere 20 μL di RNasi A nella provetta da centrifuga, mescolare sottosopra e incubare a 65 gradi per 15 minuti, mescolando sottosopra ogni 5 minuti.
2. Aggiungere 100 μl di tampone PGL2 alla provetta da centrifuga, mescolare bene e riporre in ghiaccio per 5 minuti.
3. Centrifugare a 12,000 giri al minuto per 5 minuti a 4 gradi, trasferire il surnatante in una nuova provetta da centrifuga priva di nucleasi da 2,0 mL (se è ancora presente materiale fluttuante nel surnatante ottenuto, è necessario centrifugare nuovamente a 12,000 giri al minuto per 5 minuti a 4 gradi e trasferire il surnatante in altri 2,0 mL Provetta da centrifuga priva di nucleasi, nota: il surnatante ottenuto non deve superare i 500 μL).
4. Aggiungere Buffer GB della stessa quantità di volume di liquido surnatante al surnatante della fase precedente, capovolgerlo completamente e mescolare bene.
5. Aggiungere lo stesso volume di isopropanolo alla miscela del passaggio precedente, completamente capovolto e mescolare bene. Quindi aggiungere 40 μL di SweMag Beads (le SweMag Beads devono essere disperse uniformemente prima dell'uso) e mescolare bene con una pipetta o un'oscillazione vortex.
6. Lasciare a temperatura ambiente per 10 minuti e durante il processo di posizionamento, utilizzare la pipetta per soffiare o agitare nel vortex per mescolare più volte per mantenere le SweMag Beads in sospensione.
7. Trasferire la provetta da centrifuga sul supporto magnetico e lasciarla riposare per 30 s. Quando il surnatante è limpido, aspirare ed eliminare il surnatante.
8. Aggiungere 600 μL di Buffer GD, rimuovere il supporto magnetico, utilizzare una pipetta per soffiare o agitare nel vortex finché le SweMag Beads non sono ben disperse. Trasferire la provetta da centrifuga sul supporto magnetico e lasciarla riposare per 30 s. Quando il surnatante è limpido, aspirare ed eliminare il surnatante.
9. Aggiungere 700 μL di Buffer PW, rimuovere il supporto magnetico, utilizzare una pipetta per soffiare o agitare nel vortex finché le SweMag Beads non sono ben disperse. Trasferire la provetta da centrifuga sul supporto magnetico e lasciarla riposare per 30 s. Quando il surnatante è limpido, aspirare ed eliminare il surnatante.
10. Ripetere il passaggio 9.
11. Aprire il tappo della provetta da centrifuga e lasciarla a temperatura ambiente per 5-10 minuti, in modo che l'etanolo residuo possa evaporare completamente (evitare un'essiccazione eccessiva delle SweMag Beads, che potrebbe influenzare la resa dell'acido nucleico).
12. Rimuovere il supporto magnetico, aggiungere 80-100 μL di tampone TE o acqua priva di nucleasi alla provetta da centrifuga, utilizzare una pipetta per soffiare delicatamente o agitare nel vortex finché le sfere SweMag non sono ben disperse. Lasciare a temperatura ambiente per 5 minuti.
13. Trasferire la provetta da centrifuga sul supporto magnetico finché le sfere SweMag non sono state completamente assorbite e assorbire il surnatante in una nuova provetta da centrifuga priva di nucleasi da 1,5 mL per ottenere DNA ad elevata purezza.
Nota
1. Leggere attentamente il manuale del prodotto prima dell'uso.
2. Provare a utilizzare tessuto vegetale fresco per garantire la resa e l'integrità del DNA genomico.
3. I campioni di piante crioconservati dovrebbero evitare ripetuti congelamenti e scongelamenti, altrimenti la qualità e la resa del DNA estratto saranno ridotte.
4. Per i tessuti vegetali con elevato contenuto di acido nucleico, la quantità iniziale di campioni di tessuto vegetale può essere opportunamente ridotta per renderli completamente lisati; per campioni con basso contenuto di acidi nucleici, la quantità iniziale di campioni di tessuto vegetale può essere opportunamente aumentata per ottenere una maggiore concentrazione di DNA genomico.
5. Evitare il congelamento delle sospensioni di sfere magnetiche durante la conservazione. Le sfere magnetiche sono facili da depositare e devono essere completamente vortexate prima dell'uso per mantenerle in sospensione uniforme.
6. Prima di aggiungere le sfere magnetiche al campione, i reagenti nel campione devono essere miscelati bene.
7. L'etanolo deve essere completamente evaporato prima dell'eluizione del DNA per evitare l'influenza dell'etanolo residuo sugli esperimenti successivi.
8. Non asciugare a lungo le sfere magnetiche per evitare di compromettere l'efficienza dell'eluizione del DNA.
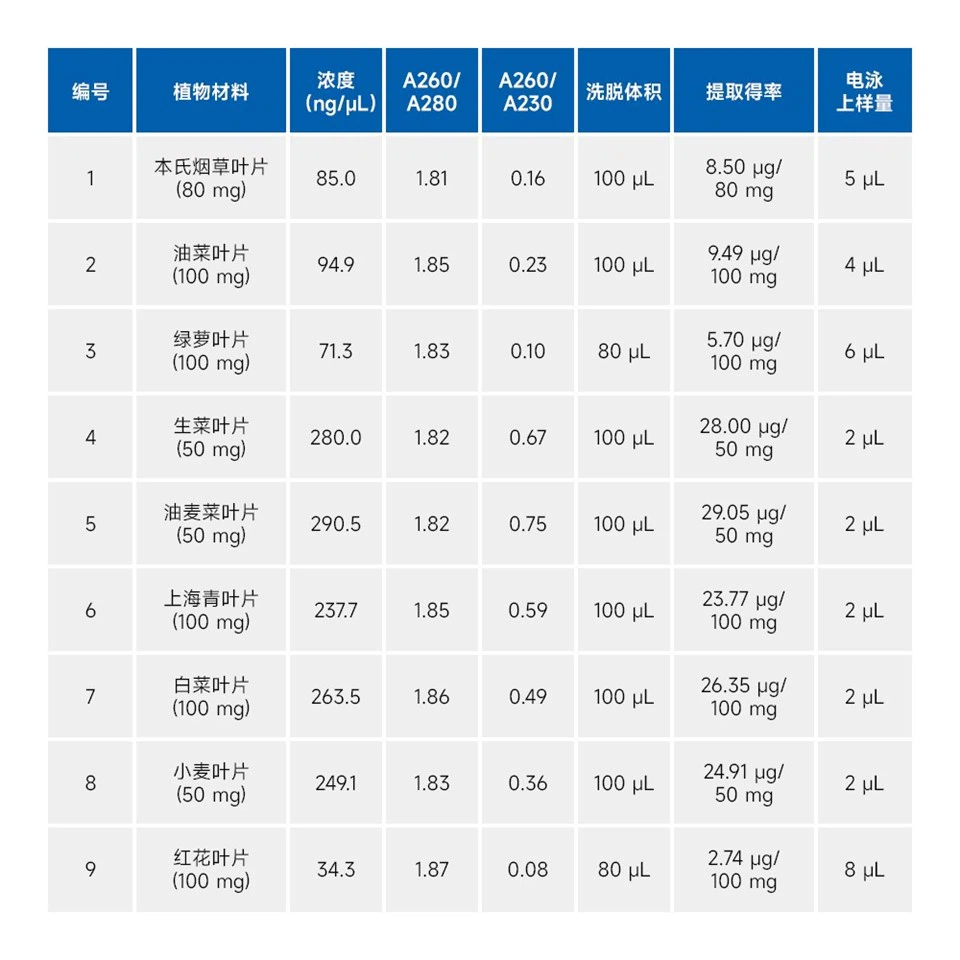
Programma
La resa del DNA genomico estratto da molti semplici campioni di piante mediante questo kit è mostrata nella tabella seguente. La resa del DNA genomico è correlata alle specie vegetali, agli organi e allo stato di crescita. La tabella seguente è solo di riferimento.
|
Nome del campione |
Dimensione del campione |
Resa del DNA |
|
Foglia di Triticum aestivum |
50 mg |
{} ug |
|
Foglia di Nicotiana benthamiana |
80 mg |
{} ug |
|
Foglia di Carthamus tinctorius |
100 mg |
{} ug |
|
Foglia di Brassica napus |
100 mg |
{} ug |
|
Foglia di Epipremnum aureum |
100 mg |
{} ug |
|
Lactuca sativa L. var. foglia ramosa |
100 mg |
{} ug |
|
Foglia di Lactuca sativa |
100 mg |
{} ug |
|
Foglia di Brassica chinensis |
100 mg |
{} ug |
|
Foglia di Brassica pekinensis |
100 mg |
ug |
Solo per uso di ricerca!
Etichetta sexy: Kit di estrazione del DNA genomico della pianta magbind, produttori di kit di estrazione del dna genomico della pianta magbind, fornitori, fabbrica